よむ、つかう、まなぶ。
資料3-2 抗がんWG (3 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198856_00024.html |
| 出典情報 | 医療上の必要性の高い未承認薬・適応外薬検討会議(第52回 8/31)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
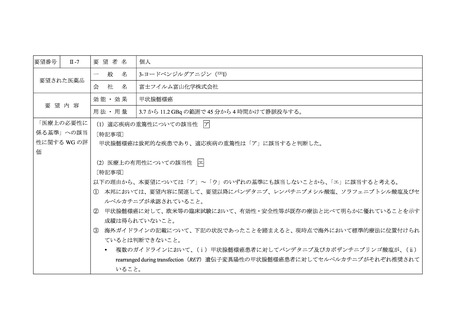
開発要請後に公表された一部の診療ガイドライン(Thyroid 2015: 25; 567-610)において、3-ヨードベンジルグアニジン(131I)
(以下、
「131I-MIBG」
)による治療は甲状腺髄様癌患者に対して有効性が認められず、放射性同位体に基づく治療は臨床試
験等の限られた状況のみにおいて考慮されるべきである旨が記載されており、その他の診療ガイドラインにおいても 131IMIBG 投与を推奨する旨の記載は認められなかったこと。
本要望については、2012年12月26日に開催された第14回医療上の必要性の高い未承認薬・適応外薬検討会議において、適応疾病の
重篤性は「ア」、医療上の有用性は「ウ」に該当し、医療上の必要性が高い旨が報告され、開発要請がなされた。
備
考
今般、開発要請時から医療環境の変化があったこと等を踏まえ、「医療上の必要性の高い未承認薬・適応外薬の要望対象の拡大に
ついて」(平成27年7月1日付け医政研発0701第2号、薬食審査発0701第2号)の記 第2の5における規定に基づき、富士フイルム富山
化学株式会社より医療上の必要性の再検討の依頼がなされたため、医療上の必要性の再検討を行った。
開発要請後に公表された一部の診療ガイドライン(Thyroid 2015: 25; 567-610)において、3-ヨードベンジルグアニジン(131I)
(以下、
「131I-MIBG」
)による治療は甲状腺髄様癌患者に対して有効性が認められず、放射性同位体に基づく治療は臨床試
験等の限られた状況のみにおいて考慮されるべきである旨が記載されており、その他の診療ガイドラインにおいても 131IMIBG 投与を推奨する旨の記載は認められなかったこと。
本要望については、2012年12月26日に開催された第14回医療上の必要性の高い未承認薬・適応外薬検討会議において、適応疾病の
重篤性は「ア」、医療上の有用性は「ウ」に該当し、医療上の必要性が高い旨が報告され、開発要請がなされた。
備
考
今般、開発要請時から医療環境の変化があったこと等を踏まえ、「医療上の必要性の高い未承認薬・適応外薬の要望対象の拡大に
ついて」(平成27年7月1日付け医政研発0701第2号、薬食審査発0701第2号)の記 第2の5における規定に基づき、富士フイルム富山
化学株式会社より医療上の必要性の再検討の依頼がなされたため、医療上の必要性の再検討を行った。