よむ、つかう、まなぶ。
参考資料8 ワクチンの副反応に対する考え方及び評価について(令和3年2月15日合同部会資料3) (11 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000208910_00043.html |
| 出典情報 | 第80回厚生科学審議会予防接種・ワクチン分科会副反応検討部会、令和4年度第5回薬事・食品衛生審議会薬事分科会医薬品等安全対策部会安全対策調査会(合同開催)(6/10)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
副反応疑い報告の収集と評価について
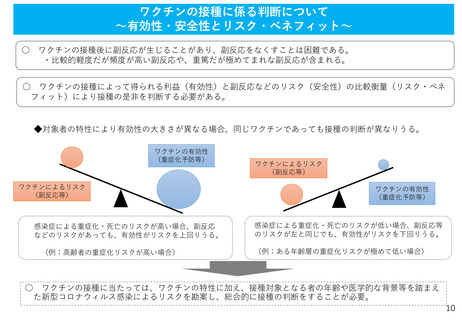
○ 医療機関等は、予防接種による副反応疑いを知ったときは、予防接種後副反応疑い報告制度に則り、専用の様式
を用いて、(独)医薬品医療機器総合機構に報告する。
○ 一方、医療機関からの報告内容のみでは、因果関係に関する評価を実施することは困難な場合もあるため、詳細
調査が行われるものの、因果関係の評価のためには、一定の期間が必要である。
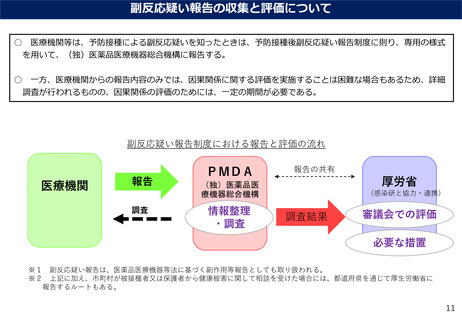
副反応疑い報告制度における報告と評価の流れ
医療機関
報告
調査
PMDA
報告の共有
厚労省
(独)医薬品医
療機器総合機構
情報整理
・調査
(感染研と協力・連携)
調査結果
審議会での評価
必要な措置
※1 副反応疑い報告は、医薬品医療機器等法に基づく副作用等報告としても取り扱われる。
※2 上記に加え、市町村が被接種者又は保護者から健康被害に関して相談を受けた場合には、都道府県を通じて厚生労働省に
報告するルートもある。
11
○ 医療機関等は、予防接種による副反応疑いを知ったときは、予防接種後副反応疑い報告制度に則り、専用の様式
を用いて、(独)医薬品医療機器総合機構に報告する。
○ 一方、医療機関からの報告内容のみでは、因果関係に関する評価を実施することは困難な場合もあるため、詳細
調査が行われるものの、因果関係の評価のためには、一定の期間が必要である。
副反応疑い報告制度における報告と評価の流れ
医療機関
報告
調査
PMDA
報告の共有
厚労省
(独)医薬品医
療機器総合機構
情報整理
・調査
(感染研と協力・連携)
調査結果
審議会での評価
必要な措置
※1 副反応疑い報告は、医薬品医療機器等法に基づく副作用等報告としても取り扱われる。
※2 上記に加え、市町村が被接種者又は保護者から健康被害に関して相談を受けた場合には、都道府県を通じて厚生労働省に
報告するルートもある。
11