よむ、つかう、まなぶ。
総-9先進医療会議からの報告について (1 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_71462.html |
| 出典情報 | 中央社会保険医療協議会 総会(第648回 3/11)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
中医協 総-9
8. 3. 11
先進医療の科学的評価結果についての報告
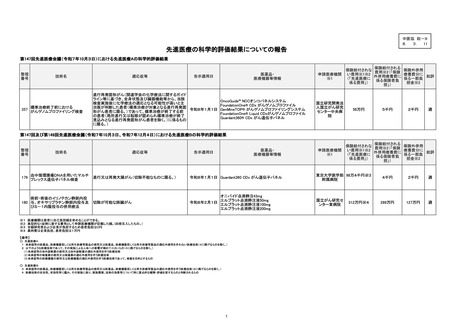
第147回先進医療会議(令和7年10月3日)における先進医療Aの科学的評価結果
整理
番号
357
技術名
標準治療終了前における
がんゲノムプロファイリング検査
適応症等
医薬品・
医療機器等情報
告示適用日
進行再発固形がん(関連学会の化学療法に関するガイド
ライン等に基づき、全身状態及び臓器機能等から、当該
OncoGuide™ NCCオンコパネルシステム
検査実施後に化学療法の適応となる可能性が高いと主
FoundationOne® CDx がんゲノムプロファイル
治医が判断した患者(標準治療が対象となる進行再発固
令和8年1月1日 GenMineTOP® がんゲノムプロファイリングシステム
形がん患者に限る。)であって、標準治療が終了する前
FoundationOne® Liquid CDxがんゲノムプロファイル
の患者(局所進行又は転移が認められ標準治療が終了
Guardant360® CDx がん遺伝子パネル
見込みとなる進行再発固形がん患者を除く。)に係るもの
に限る。)
申請医療機関
※1
国立研究開発法
人国立がん研究
センター中央病
院
保険給付される
保険給付されな
保険外併用
費用※2(「保険
い費用※1※2
療養費分に
外併用療養費に
総評
(「先進医療に
係る一部負
係る保険者負
係る費用」)
担金※2
担」)
56万円
5千円
2千円
適
第147回及び第149回先進医療会議(令和7年10月3日、令和7年12月4日)における先進医療Bの科学的評価結果
整理
番号
技術名
179
血中循環腫瘍DNAを用いたマルチ
プレックス遺伝子パネル検査
術前・術後のイリノテカン静脈内投
180 与、オキサリプラチン静脈内投与及
びS-1内服投与の併用療法
適応症等
医薬品・
医療機器等情報
告示適用日
申請医療機関
※1
保険給付される
保険給付されな
保険外併用
費用※2(「保険
い費用※1※2
療養費分に
外併用療養費に
総評
(「先進医療に
係る一部負
係る保険者負
係る費用」)
担金※2
担」)
進行又は再発大腸がん(切除不能なものに限る。)
令和8年1月1日 Guardant360 CDx がん遺伝子パネル
東京大学医学部 98万4千円※3
附属病院
4千円
2千円
適
切除が可能な膵臓がん
オニバイド点滴静注43mg
エルプラット点滴静注液50mg
令和8年2月1日
エルプラット点滴静注液100mg
エルプラット点滴静注液200mg
国立がん研究セ
ンター東病院
289万円
127万円
適
※1 医療機関は患者に自己負担額を求めることができる。
※2 典型的な1症例に要する費用として申請医療機関が記載した額。(四捨五入したもの。)
※3 全額研究者および企業が負担するため患者負担は0円
※4 薬剤費は企業負担、患者負担は1万円
【備考】
○ 先進医療A
1 未承認等の医薬品、医療機器若しくは再生医療等製品の使用又は医薬品、医療機器若しくは再生医療等製品の適応外使用を伴わない医療技術(4に掲げるものを除く。)
2 以下のような医療技術であって、その実施による人体への影響が極めて小さいもの(4に掲げるものを除く。)
(1)未承認等の体外診断薬の使用又は体外診断薬の適応外使用を伴う医療技術
(2)未承認等の検査薬の使用又は検査薬の適応外使用を伴う医療技術
(3)未承認等の医療機器の使用又は医療機器の適応外使用を伴う医療技術であって、検査を目的とするもの
○ 先進医療B
3 未承認等の医薬品、医療機器若しくは再生医療等製品の使用又は医薬品、医療機器若しくは再生医療等製品の適応外使用を伴う医療技術(2に掲げるものを除く。)
4 医療技術の安全性、有効性等に鑑み、その実施に係り、実施環境、技術の効果等について特に重点的な観察・評価を要するものと判断されるもの
1
312万円※4
8. 3. 11
先進医療の科学的評価結果についての報告
第147回先進医療会議(令和7年10月3日)における先進医療Aの科学的評価結果
整理
番号
357
技術名
標準治療終了前における
がんゲノムプロファイリング検査
適応症等
医薬品・
医療機器等情報
告示適用日
進行再発固形がん(関連学会の化学療法に関するガイド
ライン等に基づき、全身状態及び臓器機能等から、当該
OncoGuide™ NCCオンコパネルシステム
検査実施後に化学療法の適応となる可能性が高いと主
FoundationOne® CDx がんゲノムプロファイル
治医が判断した患者(標準治療が対象となる進行再発固
令和8年1月1日 GenMineTOP® がんゲノムプロファイリングシステム
形がん患者に限る。)であって、標準治療が終了する前
FoundationOne® Liquid CDxがんゲノムプロファイル
の患者(局所進行又は転移が認められ標準治療が終了
Guardant360® CDx がん遺伝子パネル
見込みとなる進行再発固形がん患者を除く。)に係るもの
に限る。)
申請医療機関
※1
国立研究開発法
人国立がん研究
センター中央病
院
保険給付される
保険給付されな
保険外併用
費用※2(「保険
い費用※1※2
療養費分に
外併用療養費に
総評
(「先進医療に
係る一部負
係る保険者負
係る費用」)
担金※2
担」)
56万円
5千円
2千円
適
第147回及び第149回先進医療会議(令和7年10月3日、令和7年12月4日)における先進医療Bの科学的評価結果
整理
番号
技術名
179
血中循環腫瘍DNAを用いたマルチ
プレックス遺伝子パネル検査
術前・術後のイリノテカン静脈内投
180 与、オキサリプラチン静脈内投与及
びS-1内服投与の併用療法
適応症等
医薬品・
医療機器等情報
告示適用日
申請医療機関
※1
保険給付される
保険給付されな
保険外併用
費用※2(「保険
い費用※1※2
療養費分に
外併用療養費に
総評
(「先進医療に
係る一部負
係る保険者負
係る費用」)
担金※2
担」)
進行又は再発大腸がん(切除不能なものに限る。)
令和8年1月1日 Guardant360 CDx がん遺伝子パネル
東京大学医学部 98万4千円※3
附属病院
4千円
2千円
適
切除が可能な膵臓がん
オニバイド点滴静注43mg
エルプラット点滴静注液50mg
令和8年2月1日
エルプラット点滴静注液100mg
エルプラット点滴静注液200mg
国立がん研究セ
ンター東病院
289万円
127万円
適
※1 医療機関は患者に自己負担額を求めることができる。
※2 典型的な1症例に要する費用として申請医療機関が記載した額。(四捨五入したもの。)
※3 全額研究者および企業が負担するため患者負担は0円
※4 薬剤費は企業負担、患者負担は1万円
【備考】
○ 先進医療A
1 未承認等の医薬品、医療機器若しくは再生医療等製品の使用又は医薬品、医療機器若しくは再生医療等製品の適応外使用を伴わない医療技術(4に掲げるものを除く。)
2 以下のような医療技術であって、その実施による人体への影響が極めて小さいもの(4に掲げるものを除く。)
(1)未承認等の体外診断薬の使用又は体外診断薬の適応外使用を伴う医療技術
(2)未承認等の検査薬の使用又は検査薬の適応外使用を伴う医療技術
(3)未承認等の医療機器の使用又は医療機器の適応外使用を伴う医療技術であって、検査を目的とするもの
○ 先進医療B
3 未承認等の医薬品、医療機器若しくは再生医療等製品の使用又は医薬品、医療機器若しくは再生医療等製品の適応外使用を伴う医療技術(2に掲げるものを除く。)
4 医療技術の安全性、有効性等に鑑み、その実施に係り、実施環境、技術の効果等について特に重点的な観察・評価を要するものと判断されるもの
1
312万円※4