よむ、つかう、まなぶ。
(先-3)[80KB]3 先進医療Bの試験終了に伴う取下げについて (1 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000205617_00110.html |
| 出典情報 | 先進医療会議(第148回 11/6)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
先ー3
7.11.6
第180回先進医療技術審査部会
令和7年10月10日
資料9
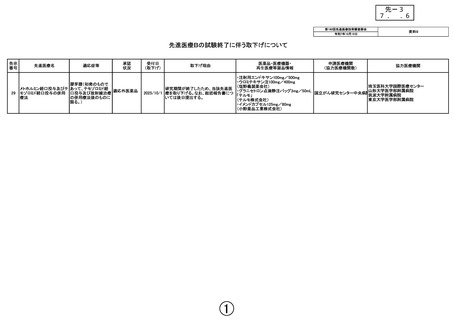
先進医療Bの試験終了に伴う取下げについて
新規申請技術の評価結果
告示
番号
29
先進医療名
適応症等
承認
状況
膠芽腫(初発のもので
メトホルミン経口投与及びテ あって、テモゾロミド経
適応外医薬品
モゾロミド経口投与の併用 口投与及び放射線治療
療法
の併用療法後のものに
限る。)
受付日
(取下げ)
医薬品・医療機器・
再生医療等製品情報
取下げ理由
申請医療機関
(協力医療機関数)
協力医療機関
・注射用エンドキサン100mg/500mg
・ウロミテキサン注100mg/400mg
埼玉医科大学国際医療センター
(塩野義製薬会社)
研究期間が終了したため、当該先進医
山形大学医学部附属病院
・グラニセトロン点滴静注バッグ3mg/50mL
2025/10/1 療を取り下げる。なお、総括報告書につ
国立がん研究センター中央病院筑波大学附属病院
「テルモ」
いては後日提出する。
東京大学医学部附属病院
(テルモ株式会社)
・イメンドカプセル125mg/80mg
(小野薬品工業株式会社)
1
7.11.6
第180回先進医療技術審査部会
令和7年10月10日
資料9
先進医療Bの試験終了に伴う取下げについて
新規申請技術の評価結果
告示
番号
29
先進医療名
適応症等
承認
状況
膠芽腫(初発のもので
メトホルミン経口投与及びテ あって、テモゾロミド経
適応外医薬品
モゾロミド経口投与の併用 口投与及び放射線治療
療法
の併用療法後のものに
限る。)
受付日
(取下げ)
医薬品・医療機器・
再生医療等製品情報
取下げ理由
申請医療機関
(協力医療機関数)
協力医療機関
・注射用エンドキサン100mg/500mg
・ウロミテキサン注100mg/400mg
埼玉医科大学国際医療センター
(塩野義製薬会社)
研究期間が終了したため、当該先進医
山形大学医学部附属病院
・グラニセトロン点滴静注バッグ3mg/50mL
2025/10/1 療を取り下げる。なお、総括報告書につ
国立がん研究センター中央病院筑波大学附属病院
「テルモ」
いては後日提出する。
東京大学医学部附属病院
(テルモ株式会社)
・イメンドカプセル125mg/80mg
(小野薬品工業株式会社)
1