よむ、つかう、まなぶ。
○令和 6 年度薬価 制度改革 の骨子( たたき台 )について 薬-2 (4 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000212451_00084.html |
| 出典情報 | 中央社会保険医療協議会 薬価専門部会(第220回 12/13)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
新薬創出等加算の対象企業の考え方(対応案)①
薬価算定の基準
第9節 新薬創出・適応外薬解消等促進加算
1
加算
(1)対象品目
(略)
(2)対象企業
新薬創出等加算の対象企業は、未承認薬等検討会議における検討結果を踏まえ、厚生労働省から開発を要請された品目について、
開発の拒否、合理的な理由のない開発の遅延等、適切に対応を行わなかった企業以外の企業とする。
(3)薬価の改定方式
(1)に該当する品目については、(2)に掲げる企業が製造販売するものに限り、本規定の適用前の価格に、別表11※に定める
額を加えた額に改定する。
(対応案)新薬の薬価を維持した費用を研究開発の投資に活用したことを判断する
ため、対象企業に以下の考え方を追加。
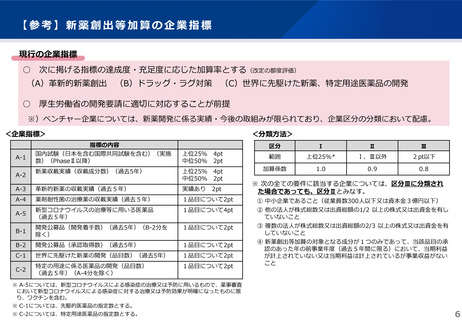
確認事項(過去5年の実績)
A-1
国内試験(日本を含む国際共同試験を含む)(実施数)
(PhaseⅡ以降)
A-2
新薬収載実績(収載成分数)
⚫ 国内での新薬開発を一定期間行っていない企業も対象外とする
A-3
革新性のある新薬の収載実績(収載成分数)
⚫ 判断基準は現行の加算係数の判断に用いている企業指標の項目を用いる。(企業
指標のポイント状況は今後も把握して、今回の新創加算見直しの検証としても用
いる)
A-4
薬剤耐性菌の治療薬の収載実績(収載成分数)
A-5
新型コロナウイルスの治療等に用いる医薬品の開発実績
(承認取得数)
B-1
開発公募品(開発着手数)(B-2分を除く)
B-2
開発公募品(承認取得数)
C-1
世界に先駆けた新薬の開発(品目数)
C-2
特定の用途に係る医薬品の開発(品目数)
(A-4分を除く)
⇒ 過去5年間、企業指標のどれも満たさない場合は除外(現行のA-1、A-2は相対的
なポイント制であるが、該当する品目があれば要件を満たすこととする)
4
薬価算定の基準
第9節 新薬創出・適応外薬解消等促進加算
1
加算
(1)対象品目
(略)
(2)対象企業
新薬創出等加算の対象企業は、未承認薬等検討会議における検討結果を踏まえ、厚生労働省から開発を要請された品目について、
開発の拒否、合理的な理由のない開発の遅延等、適切に対応を行わなかった企業以外の企業とする。
(3)薬価の改定方式
(1)に該当する品目については、(2)に掲げる企業が製造販売するものに限り、本規定の適用前の価格に、別表11※に定める
額を加えた額に改定する。
(対応案)新薬の薬価を維持した費用を研究開発の投資に活用したことを判断する
ため、対象企業に以下の考え方を追加。
確認事項(過去5年の実績)
A-1
国内試験(日本を含む国際共同試験を含む)(実施数)
(PhaseⅡ以降)
A-2
新薬収載実績(収載成分数)
⚫ 国内での新薬開発を一定期間行っていない企業も対象外とする
A-3
革新性のある新薬の収載実績(収載成分数)
⚫ 判断基準は現行の加算係数の判断に用いている企業指標の項目を用いる。(企業
指標のポイント状況は今後も把握して、今回の新創加算見直しの検証としても用
いる)
A-4
薬剤耐性菌の治療薬の収載実績(収載成分数)
A-5
新型コロナウイルスの治療等に用いる医薬品の開発実績
(承認取得数)
B-1
開発公募品(開発着手数)(B-2分を除く)
B-2
開発公募品(承認取得数)
C-1
世界に先駆けた新薬の開発(品目数)
C-2
特定の用途に係る医薬品の開発(品目数)
(A-4分を除く)
⇒ 過去5年間、企業指標のどれも満たさない場合は除外(現行のA-1、A-2は相対的
なポイント制であるが、該当する品目があれば要件を満たすこととする)
4